高级别浆液性卵巢癌(HGSOC)是最致命的妇科恶性肿瘤,它与肿瘤间质密切相互作用,生长迅速,广泛转移,并表现出侵袭性病程。目前的标准治疗包括手术、化疗、单克隆抗体,以及PARP抑制剂。然而,约70%的患者在手术和化疗后3年内复发,并死于疾病进展。这种情况在最近20年里几乎没有得到改善。
TP53(表达p53蛋白)基因突变是人类癌症中最常见的基因突变,癌症基因组图谱研究网络揭示,高达96%的HGSOC病例以失活或截短的TP53为特征。此外,TP53突变似乎发生在卵巢癌早期,这支持了突变TP53作为这种恶性肿瘤驱动因素。
近日,法兰克福大学的研究人员在 Cancer Communications 期刊发表了题为:Rescue of p53 functions by in vitro-transcribed mRNA impedes the growth of high-grade serous ovarian cancer 的研究论文。

在96%的高级别浆液性卵巢癌(HGSOC)患者中存在着相同的临床表现——抑癌基因TP53发生突变。TP53基因表达的p53蛋白能够识别并修复细胞中的DNA损伤,当损伤无法修复时则诱导细胞死亡,从而防止异常细胞增殖,预防癌症发生。当TP53基因突变时,产生的突变p53蛋白失去了抑癌作用。
在这项研究中,研究团队尝试使用mRNA来恢复正常的p53蛋白表达。他们在实验室中合成了编码正确p53蛋白的mRNA,让后将其装载到脂质体中进行递送,其可在各种人类癌细胞系中表达功能性的p53蛋白。
接下来,研究团队从法兰克福大学医院获取了来自卵巢癌患者的肿瘤样本,并构建了患者来源的卵巢癌类器官,在接受上述mRNA治疗后,这些患者来源的卵巢癌类器官开始萎缩并死亡。
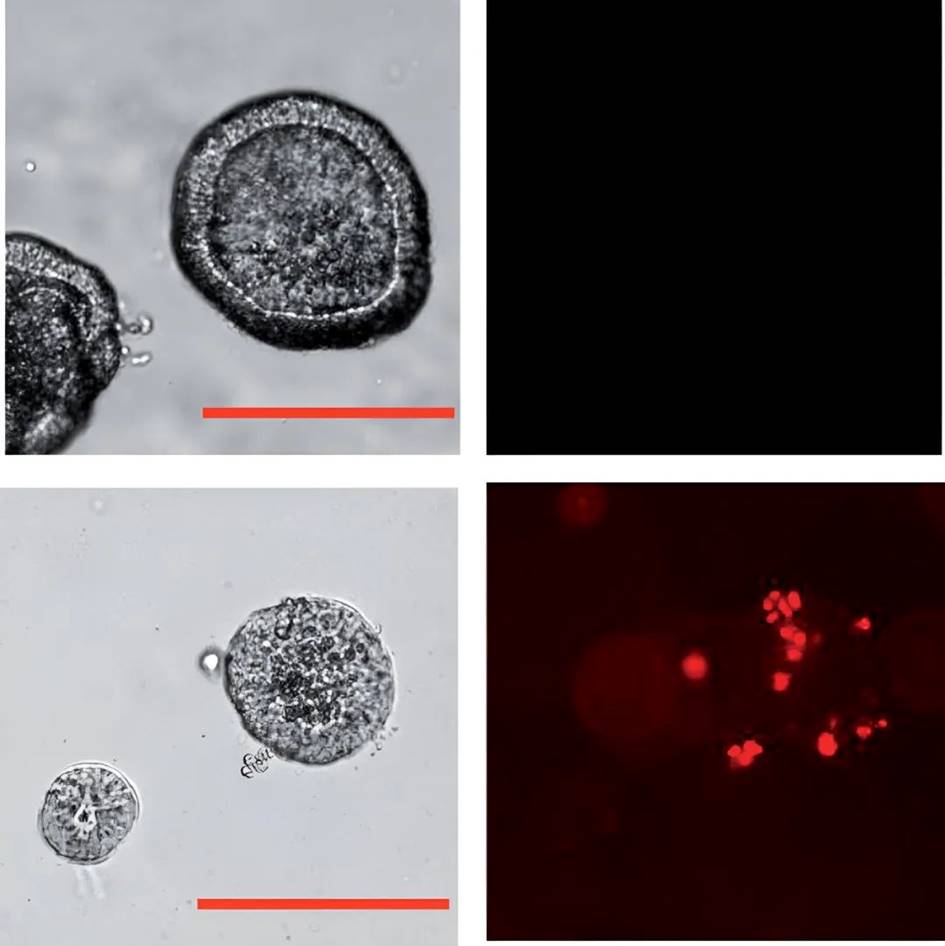
患者来源的卵巢癌类器官(上图)在p53 mRNA治疗后萎缩并死亡(下图)
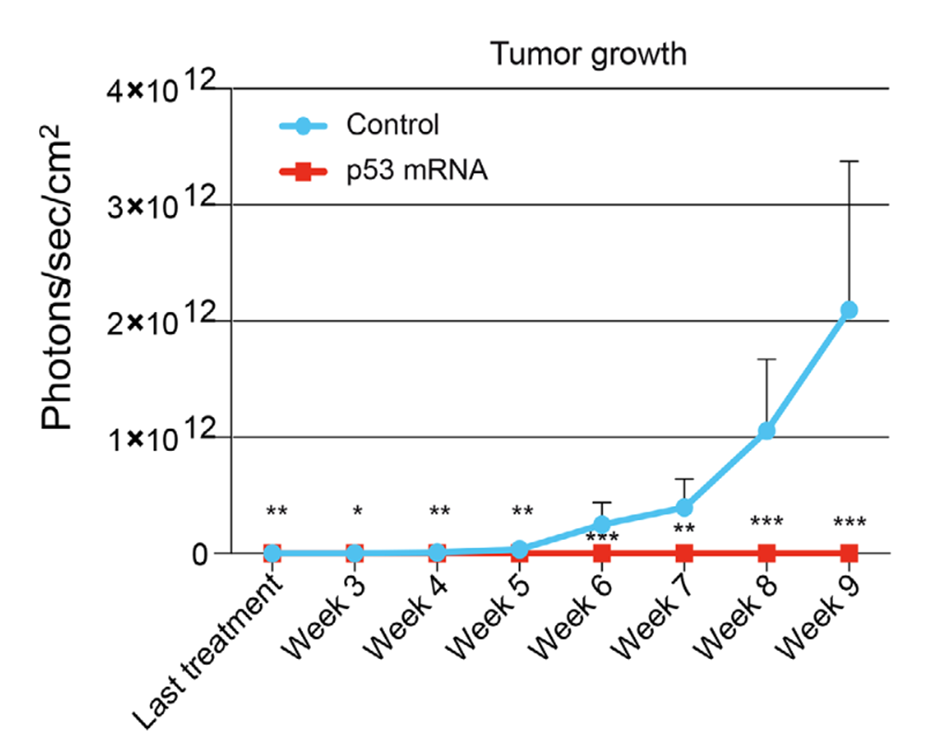
为了进一步测试该mRNA疗法是否在体内有效,并能对抗卵巢癌的腹部转移,研究团队将人类卵巢肿瘤细胞植入小鼠的卵巢中,构建了卵巢癌小鼠模型,并在一段时间后向这些小鼠体内注射了mRNA脂质体。
结果显示,这些mRNA在小鼠模型体内产生了大量功能性p53蛋白,它们卵巢中的肿瘤和转移几乎完全消失了。
研究同意的表示,这项研究中的mRNA疗法之所以如此成功,部分原因是mRNA技术的进步,通过对mRNA的修饰,大大延长了其寿命,该研究中的mRNA可在小鼠体内表达两周之久。此外,经过修饰的mRNA没有引发炎症反应。
总的来说,这项研究表明,使用mRNA在体内表达p53蛋白有望成为高级别浆液性卵巢癌(HGSOC)的潜在治疗策略,也为p53功能的分子机制及其在卵巢癌治疗中的相关性提供了有价值的见解。
论文链接:
https://onlinelibrary.wiley.com/doi/10.1002/cac2.12511
来源:生物世界













